[코스인코리아닷컴 김세화 기자] 유로핀즈 C&PC(Eurofins Cosmetic & Personal Care)가 7월 9일 오전 10시부터 12시까지 '미용기기의 임상시험과 의료기기 규제 전략'을 주제로 온라인 웨비나를 개최했다. 이날 웨비나에는 미용기기, 기능성화장품 제조업체, 의료기기 스타트업, RA, R&D, 마케팅, 임상기획 실무자 등 120여 명이 참석해 규제 변화에 따른 대응 전략을 논의했다.
이번 웨비나에는 화장품 및 퍼스널케어 제품의 안전성, 효능, 품질 평가를 전문적으로 수행하는 글로벌 시험·분석 기관 유로핀즈와, 의료기기 및 뷰티 디바이스 분야에서 글로벌 인허가·규제 컨설팅을 제공하는 이머고 by UL(Emergo by UL)의 전문가가 참여해 해당 분야의 최신 정보를 공유했다.

첫 번째 발표는 임재욱 유로핀즈 C&PC 이사가 '기능성화장품과 미용기기의 임상시험 전략'에 대해 발표했다.
이날 임 이사는 한국, 유럽, 미국 등 주요국의 분류 기준과 규제 차이를 비교하며 "제품의 작용 메커니즘과 표현 방식에 따라 의료기기로 간주될 수 있는 리스크가 발생할 수 있다"고 강조하며, 국가별 규제 기준에 따른 클레임 전략의 중요성을 강조했다. 특히 미국의 경우, 생리적 기능 변화를 동반하는 디바이스는 의료기기로 분류된다는 점을 짚으며, 기업이 제품 기획 단계에서부터 각국의 기준을 면밀히 분석해야 한다고 지적했다.
이어 유럽, 미국, 아시아 지역의 글로벌 임상시험 사례와 설계 결과를 공유하며, 유로핀즈의 글로벌 네트워크를 활용한 인체적용시험과 사용성 평가의 병행 방안이 소개됐다.
그는 "임상 목적에 따라 시험 방식을 달리해야 한다"며 "특히 인체적용시험은 과학적 근거 확보와 법적 효능 표시를 위한 핵심 전략으로 고정밀 장비와 전문가의 평가가 수반돼야 한다"고 설명했다. 반면 사용성 평가는 소비자 중심의 설문·인터뷰 기반으로 마케팅 자료로 활용도가 높지만, 법적 클레임에 사용할 수 있는 과학적 데이터 확보에는 한계가 있다고 덧붙였다.
임상시험 전략

임 이사는 "글로벌 시장 진출을 위한 임상시험 전략의 핵심은 각국 규제 요구에 부합하는 맞춤형 데이터 확보와 초기 단계에서의 방향성 설정"이라며 "임상 담당자와 해외 진출 기업이 클레임 리스크를 사전에 파악하고, 허용된 표현만 사용하는 것이 중요하다"고 강조했다.
광고 규제와 관련해서는 피부 탄력 개선, 주름 제거, 콜라겐 생성 촉진 등 주요 클레임별로 국가별 규제 기준과 광고 리스크를 상세히 분석하며, 표현 하나로도 규제 대상이 될 수 있다고 지적했다. 나라별로는 한국의 경우, 의료기기 광고에 사전 심의가 필수이며 미용기기 역시 의료적 표현 사용 시 규제 대상이 될 수 있다.
유럽은 △공정성 △진실성 △증거 기반 △소비자 판단 지원이라는 네 가지 원칙을 광고의 기준으로 적용하고 있으며, 미국은 식품의약국(FDA)와 연방거래위원회(FTC)의 이중 감시 체계 아래 매우 엄격한 기준이 적용된다.
임 이사는 이날 발표를 마무리하며 "제품의 목적, 작용 기전, 마케팅 전략, 각국 규제 현황을 종합적으로 고려해 의료기기와 미용기기를 명확히 구분하고, 글로벌 시장에 부합하는 맞춤형 임상시험 설계가 필요하다"고 강조했다.

두 번째 발표는 이머고 by UL의 이지운 과장이 '의료기기 인허가 및 글로벌 진출 전략'을 주제로 발표를 진행했다. 이 과장은 의료기기 규제의 흐름과 최신 동향을 소개하며 "의료기기는 화장품이나 미용기기보다 훨씬 엄격한 규제를 받아 왔다"며 "최근에는 FDA 등 해외 규제 당국의 허가를 받는 과정에서 잘못된 정보와 미흡한 준비로 어려움을 겪고 있다"고 설명했다.
이어 이 과장은 "미용기기의 특성상 의료기기로 분류될 가능성이 높기 때문에, 제품 개발 전 각국의 분류 기준과 요구 사항을 정확히 이해해야 한다"며 "1등급 제품이라도 국가별 기준에 따라 미허가 의료기기로 간주될 수 있으며, 특히 글로벌 브랜드는 현지 규제 당국의 분류 기준을 면밀히 분석해 등록 여부를 사전에 판단해야 한다"고 조언했다.
글로벌 진출 전략으로는 미국, 유럽, 일본 등 주요 시장의 제도 변화에 주목했다. 그는 "각국이 의료기기 등록을 법제화하고 있는 상황에서 기업은 생산 초기 단계부터 현지 규제에 적합한 제품 설계와 품질 시스템 구축을 병행해야 한다"며 "브라질, 일본 등 신흥 시장도 고유한 분류 및 등록 절차를 운영하고 있어, 글로벌 진출 시 국가별 세부 요건을 꼼꼼히 확인해야 한다"고 말했다.
또한 의료기기 홍보 및 판매 시에는 사용 목적과 마케팅 전략을 명확히 설정하고, 일반 사용자 대상 제품일수록 리스크 관리를 철저히 해야 하며 전문가의 의견을 충분히 반영해야 한다고 제안했다. 그는 일부 1등급 제품조차도 허가 과정에서 현지 규제 당국의 정밀한 검토가 이뤄질 수 있다는 점을 언급하며, 기업 내부의 규제 담당자 지정과 품질 시스템 확보의 중요성을 강조했다.
특히 미 FDA의 483 폼(Form FDA 483, 위반사항 통지서)를 언급하며 규제 당국의 지적에 신속하게 대응하기 위해서는 전문 컨설팅 업체의 도움을 받아 문제를 개선하고 허가 소유권, 현지 대리인 제도 등 국가별 절차를 숙지해야 한다고 강조했다. 또 브라질, 멕시코, 동남아 등 신흥 시장 진출 시에도 허가 절차, 심사 기준, 현장 실사 및 인증 요건, 수수료 등의 실무적 요소까지 사전 검토가 필수적이라고 덧붙였다.
신흥시장 인허가 전략
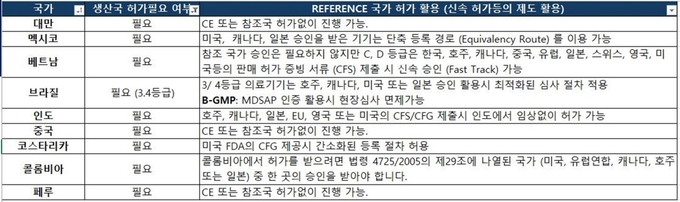
마지막으로 이 과장은 "글로벌 미용 의료기기 시장이 지속적으로 성장하고 있지만. 각국의 규제 장벽은 점점 높아지고 있으며, 인허가 절차도 복잡해지고 있는 상황"이라며, "기업들은 국가별 규제에 맞는 맞춤형 전략과 품질 시스템, 전문 컨설팅 활용을 통해 시장 진입 리스크를 최소화해야 한다"고 강조했다.
이날 웨비나를 주최한 유로핀즈 C&PC는 “이번 웨비나가 경계 제품을 다루는 기업들에게 글로벌 인허가 대응과 임상 전략 수립에 실질적인 도움을 줄 수 있었기를 바란다”며 "앞으로도 글로벌 규제 변화에 맞춰 전문성있는 웨비나를 지속적으로 제공하겠다"고 밝혔다.
Copyright ⓒ Since 2012 COS'IN. All Right Reserved.
#코스인 #코스인코리아닷컴 #화장품 #코스메틱 #유로핀스C&PC #온라인웨비나 #미용기기 #기능성화장품 #의료기기 #임상시험전략 #인허가 #글로벌진출전략 #광고리스크예방 #임상데이터활용방안 #임재욱이사 #EMERGO by UL #이지운과장 #최신정보공유 #미용기기 #기능성화장품제조업체 #의료기기스타트업 #RA #R&D #마케팅 #임상기획실무자